1月1日出版的Science报道了以色列魏茨曼科学院研究者关于m6A修饰对胚胎干细胞多能性调控作用的最新研究成果。
N6-甲基腺嘌呤(m6A)是哺乳动物mRNA中最普遍的一种RNA甲基化形式,这种修饰对mRNA剪接、运输、加工及代谢过程有重要调控作用,目前已经确认Mettl3和Mettl14两种甲基转移酶能够催化哺乳动物mRNA上产生m6A修饰。
小鼠多能性胚胎干细胞一般保持着一种原始态多能性(naive pluripotency),但在之前研究中,研究者从植入前胚胎上胚层(pre-implantation epiblast)中分离的上胚层干细胞(epiblast stem cells,EpiSCs)表现出了更高级的发育状态,甚至已经开始进入分化初始阶段。利用siRNA对原始态ESCs中转录和表观调控因子进行筛选,研究者发现EpiSCs的分化初始状态需要依赖Mettl3这个甲基转移酶。
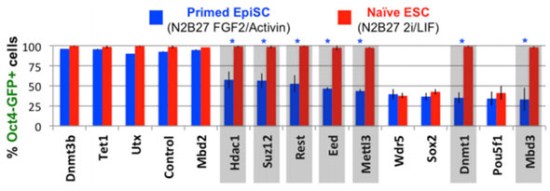
siRNA筛选ESCs中Oct4调控因子
随后,研究者将目光集中到了Mettl3所催化的m6A在EpiSCs多能性转变过程中的功能上。他们构建了一种Mettl3-/-型突变小鼠ESCs,首先利用meRIP-Seq技术对正常小鼠ESCs中m6A修饰的分布进行了检测,结果发现,有将近80%的促多能基因所转录mRNA都携带有m6A修饰,通过质谱分析发现Mettl3-/-型突变细胞中促多能基因mRNA上的m6A几乎完全消失,转录丰度明显更高,mRNA半衰期延长,翻译效率增加。这类细胞在分化培养条件下还能够一直保持正常形态,增殖产生密集的胚样小体(embryoid bodies),多种多能性标志物稳定表达,成为超多能性细胞,但WT型ESCs则随着其分化标志物的表达很快进入分化阶段。将突变ESCs注入小鼠体内,能够比正常ESCs产生更大的畸胎瘤,分化组分更少,Oct4/Nanog多能性标志物广泛表达,畸胎瘤中的细胞甚至能在6天内重新生成Oct4-GFP-ESC细胞系。
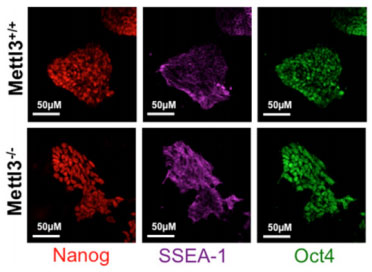
突变ESCs细胞形态及免疫组化实验结果
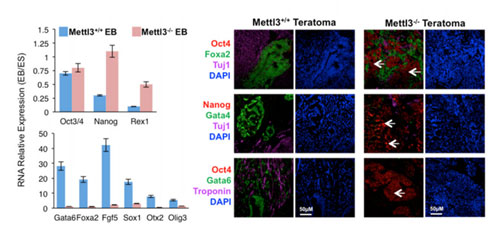
突变ESCs在小鼠体内产生畸胎瘤中促多能性基因表达量及免疫组化分析结果
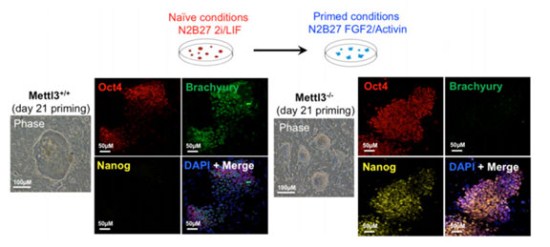
突变ESCs和野生型ESCs在分化诱导条件下培养21天后细胞形态及促多能性基因免疫组化

突变ESCs及野生型ESCs的meRIP-Seq及RNA-Seq结果,从图中可以看出,正常ESCs中带有m6A的reads在突变ESCs中丰度明显提高,表明Mettl3被沉默在降低m6A修饰水平的同时,提高了促多能性基因表达
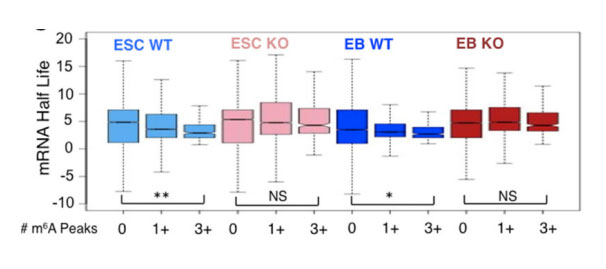
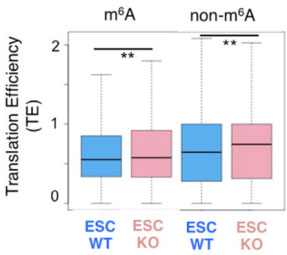
突变ESCs中促多能性基因mRNA半衰期增加,翻译效率提高
研究者使用多种RNA修饰研究技术,从体内及体外层面对m6A这种重要的RNA修饰在ESCs干性调控过程中的角色进行了探索,其结果表明m6A能够通过影响促多能性基因的mRNA水平与稳定性,对ESCs的多能性进行调控。在未来进一步的干细胞研究中,这项成果或许能够为研究者更好地控制干细胞提供有利依据,具有重要意义。
相关文献:Geula S, Moshitch-Moshkovitz S, Dominissini D, et al. m6A mRNA methylation facilitates resolution of naïve pluripotency toward differentiation[J]. Science, 2015: 1261417.